»фҒy¶ҫЛШөДҪYҳӢЎў№ҰДЬәНЦВІЎҷCЦЖј°ФЪбtҢWоIУтөД‘ӘУГ
ТэСФ
»фҒy¶ҫЛШЈЁCholera ToxinЈ¬»фҒy¶ҫЛШЈ©ЧФ°l¬FТФҒнЈ¬ЖдӘҡМШөДРФЩ|әНҸV·әөД№ҰДЬТэ°lБЛҝЖҢWҪзөДқвәсЕdИӨЎЈҸДЧоіхұ»Т•ЧчҶОјғТэ°l»фҒy°Y оөДДc¶ҫЛШЈ¬өҪИзҪсіЙһйГвТЯҢWәНбtҢWСРҫҝөДҪ№ьcЈ¬»фҒy¶ҫЛШФЪ¶аӮҖоIУтХ№¬FіцҫЮҙуөДқ“БҰЎЈ
°l¬FҡvіМ
1884 ДкЈ¬Б_І®МШ・ҝЖәХҸД°Јј°өДјSұгҳУұҫЦР·Цлxіц»фҒy»ЎҫъЈ¬ғЙДкәуЛыНЖңy»фҒy»Ўҫъ·ЦГЪөД “¶ҫЛШ” КЗТэ°lјІІЎ°Y оөДФӯТтЎЈЦұөҪ 1959 ДкЈ¬S.N. De ІЕЧCҢҚБЛ»фҒy¶ҫЛШөДҙжФЪЈ¬°l¬F»фҒy»ЎҫъөДҹoјҡ°ыЕарBһVТәДЬФЪіЙДкНГҪYФъөД»ШДcсИЦРТэ°lҙуБҝ “ГЧң«ҳУ” Тәуw·eАЫЎЈлSәуЈ¬АнІйөВ・·ТҝЛ –Л№М№өДҲFк іЙ№Ұ·ЦлxәНјғ»ҜБЛ »фҒy¶ҫЛШЈ¬ІўГчҙ_БЛЖдҒҶ»щҪYҳӢЎЈ1973 ДкЈ¬King әН van Heyningen °l¬FБЛ»фҒy¶ҫЛШөДКЬуw —— ҶОНЩТәЛбЙсҪӣ№қЬХЦ¬ GM1Ј¬һйЙоИлАнҪв»фҒy¶ҫЛШөДЧчУГҷCЦЖөм¶ЁБЛ»щөAЎЈ
»фҒy¶ҫЛШөДҪYҳӢЕcЦВІЎҷCЦЖ
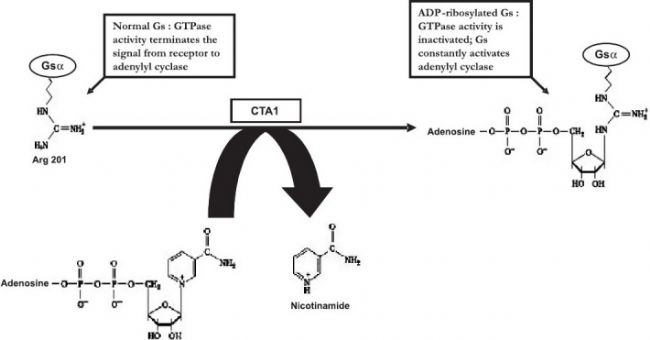
»фҒy¶ҫЛШУЙ A ҒҶ»щЈЁ240 ӮҖ°ұ»щЛбЈ¬·ЦЧУБҝ 28kDЈ©әНОеӮҖ B ҒҶ»щЈЁГҝӮҖ 103 ӮҖ°ұ»щЛбЈ¬·ЦЧУБҝ 11kDЈ¬ҝӮ·ЦЧУБҝјs 56kDЈ©ҪMіЙЎЈA ҒҶ»щУЦ·Цһй A1 әН A2 ғЙӮҖҪYҳӢУтЈ¬A1 Ш“ШҹҙЯ»Ҝ ADP - әЛМЗ»щ»ҜЈ¬A2 „tЖрөҪЯBҪУ A1 Еc B ҒҶ»щОеҫЫуwөДЧчУГЎЈ
»фҒy¶ҫЛШНЁЯ^ B ҒҶ»щЕc GM1 КЬуwҪYәПЈ¬ҪӣғИНМЧчУГЯMИлјҡ°ыЈ¬ДжРРЯ\Э”ЦБғИЩ|ҫWЎЈФЪЯ@Т»Я^іМЦРЈ¬A ҒҶ»щЕc B ҒҶ»щҪвлxЈ¬A1 ҪYҳӢУтҪиЦъғИЩ|ҫWПакPҪөҪвНҫҸҪЯMИлјҡ°ыЩ|Ј¬ҙЯ»Ҝ Gsα ҒҶ»щөД ADP - әЛМЗ»щ»ҜЈ¬К№ПЩЬХЛбӯh»ҜГёіЦАmјӨ»оЈ¬јҡ°ығИ cAMP Л®ЖҪЙэёЯЈ¬ЧоҪKҢ§ЦВВИлxЧУНвБчЎўвcлxЧУғИБчңpЙЩЈ¬ҙуБҝЛ®·ЦНЁЯ^ДcөАјҡ°ыЕЕіцЈ¬Тэ°l»фҒyөДөдРН°Y о —— ҮАЦШё№һaәНҮIНВЎЈ
»фҒy¶ҫЛШөДГвТЯХ{№қ№ҰДЬ
іэБЛЦВІЎЧчУГЈ¬»фҒy¶ҫЛШЯҖҫЯУРп@ЦшөДГвТЯХ{№қМШРФЎЈЛьҝЙТФЧчһйГвТЯЧф„©Ј¬ФцҸҠҝ№ФӯіКЯfјҡ°ыҢҰҝ№ФӯөДіКЯfДЬБҰЈ¬ҙЩЯM B јҡ°ыөДН¬·NРН·Ц»ҜЈ¬ФцјУ IgA өДРОіЙЈ¬Н¬•rЙПХ{јҡ°ыұнГж№ІҙМјӨ·ЦЧУәНЪ…»ҜТтЧУКЬуwөДұнЯ_ЎЈ
»фҒy¶ҫЛШҢҰГвТЯ‘ӘҙрөДҳOРФУ°н‘ҙжФЪ ҺЧhЈ¬УРСРҫҝұнГчЛьҝЙҙЩК№УЧЦЙ T јҡ°ыПт Th2 ұнРН·Ц»ҜЈ¬ТІУРСРҫҝ°l¬FЛьДЬХTҢ§ Th1/Th2 »мәПРНГвТЯ‘ӘҙрЎЈ
»фҒy¶ҫЛШЯҖДЬТЦЦЖСЧ°Y·ҙ‘ӘЈ¬»фҒy¶ҫЛШB оAМҺАнҫЮКЙјҡ°ыҝЙТЦЦЖ LPS ҙМјӨПВ TNFα әН NO өД®aЙъЈ¬ЖдҷCЦЖЕcХTҢ§ MAPK БЧЛбГё - 1ЈЁMKP1Ј©ұнЯ_ЎўТЦЦЖ Janus јӨГёәН p38 јӨ»оУРкPЎЈ
»фҒy¶ҫЛШФЪбtҢWоIУтөД‘ӘУГ
»щУЪ»фҒy¶ҫЛШөДЯ@Р©МШРФЈ¬ЛьФЪбtҢWоIУтХ№¬FіцБЛҸV·әөД‘ӘУГЗ°ҫ°ЎЈФЪТЯГзСР°l·ҪГжЈ¬CTB ТСұ»ј{ИлҮшлHФSҝЙөДҝЪ·ю»фҒyТЯГз DUKORAL™ЦРЈ¬Ф“ТЯГзУЙ rCTB Еcҹб»тёЈ –сRБЦңз»оөД»фҒy»Ўҫъ O1 И«јҡ°ы»мәП¶шіЙЈ¬ҪӣҙуТҺДЈЕRҙІФҮтһтһЧC°ІИ«УРР§ЎЈ
ФЪГвТЯЦОҜҹ·ҪГжЈ¬CTB ДЬХTҢ§рӨДӨГвТЯДНКЬЈ¬УГУЪЦОҜҹЧФЙнГвТЯРФјІІЎЎЈАэИзЈ¬CTB ЕcЛиЗКүAРФө°°ЧҪYәПҝЙоA·АҢҚтһРФЯ^ГфРФДXј№ЛиСЧЈ¬ЕcТИҚuЛШҪYәПДЬСУҫҸТ»Сх»ҜөӘИұПЭРЎКуТИҚuЛШТАЩҮРНМЗДтІЎөД°lІЎЈ¬ОҙҪYәПөД rCTB ТІДЬФЪ NOD РЎКуЦРХTҢ§йLЖЪөДМЗДтІЎұЈЧoЧчУГЎЈбҳҢҰ°ЧИыІЎәНҝЛБ_¶чІЎөДЕRҙІФҮтһТІіхІҪЧCҢҚБЛ CTB ЦОҜҹөД°ІИ«РФәНУРР§РФЎЈ
РЎҪY
ұM№Ь »фҒy¶ҫЛШФЪбtҢWСРҫҝЦРИЎөГБЛЦT¶аЯMХ№Ј¬ө«ҢўЖд‘ӘУГУЪИЛоҗЦОҜҹИФГжЕRМф‘рЈ¬ЦчТӘКЗЖдИ«¶ҫЛШөД¶ҫРФҶ–о}ЎЈһйҙЛЈ¬ҝЖСРИЛҶTНЁЯ^¶а·NІЯВФй_°lөН¶ҫ»тҹo¶ҫөД»фҒy¶ҫЛШСЬЙъОпЈ¬ИзЯx“сCTB ЧчһйЧф„©ЎўЯMРР¶ЁьcН»ЧғТФј°ҳӢҪЁИЪәПө°°ЧөИЈ¬ФЪҪөөН¶ҫРФөДН¬•rұЈБфЖдГвТЯХ{№қәНЧф„©»оРФЎЈ»фҒy¶ҫЛШЧчһйТ»·N¶а№ҰДЬө°°ЧЩ|Ј¬ФЪҪYҳӢЎў№ҰДЬәНбtҢW‘ӘУГ·ҪГжөДСРҫҝіЙ№ыһйОҙҒнөДГвТЯҢWәНбtҢW°lХ№МṩБЛЦШТӘөДАнХ“»щөAәНҢҚЫ`·ҪПтЎЈлSЦшСРҫҝөДІ»”аЙоИлЈ¬УРНыЯMТ»ІҪНЪҫтЖдқ“БҰЈ¬й_°lіцёь¶а°ІИ«УРР§өДЦОҜҹ·Ҫ·ЁәНТЯГзЈ¬һйИЛоҗҪЎҝөКВҳIЧціцёьҙуШ•«IЎЈ

әјЦЭЛ№Я_МШ (www.starter-bio.com)ЦҫФЪһйИ«ЗтЙъГьҝЖҢWРРҳIМṩғһЩ|өДҝ№уwЎўө°°ЧЎўФҮ„©әРөИ®aЖ·ј°СР°l·ю„ХЎЈТАНР¶аӮҖй_°lЖҪЕ_ЈәЦШҪMНГҶОҝ№ЎўЦШҪMКуҶОҝ№ЎўҝмЛЩКуҶОҝ№ЎўЦШҪMө°°Чй_°lЖҪЕ_ЈЁE.coli,CHO,HEK293,InsectCellsЈ©,ТСХэКҪНЁЯ^ҡWГЛ98/79/ECХJЧCЎўISO9001ХJЧCЎўISO13485ЎЈ
- Ni/№вСх»ҜЯҖФӯлpҙЯ»ҜЦъБҰҳӢҪЁCsp2-Csp3жI
- јҡ°ыҪЗө°°ЧҳЛУӣОпФЪ·О°©ЎўйgЖӨБцәНРШПЩБцФ\”аЦРөД‘ӘУГ
- »фҒy¶ҫЛШөДҪYҳӢЎў№ҰДЬәНЦВІЎҷCЦЖј°ФЪбtҢWоIУтөД‘ӘУГ
- К№УГStreptozotocinҳӢҪЁҙуРЎКуМЗДтІЎДЈРНөДҷCЦЖј°Жд‘ӘУГ°ёАэ
- ОўЙъОпҝмЛЩҷzңy·Ҫ·Ё·ЦоҗҪйҪB
- Ъ…»ҜТтЧУChemokinesөД·ЦоҗҪYҳӢЎў№ҰДЬј°ФЪЕRҙІЦРөД‘ӘУГ
- CEACAM6ФЪД[БцЦРөДЧчУГҷCЦЖј°°РПтЛҺОпСР°lЯMХ№
- CDX2ФЪҪYЦұДc°©°lЙъ°lХ№ЦРөДЧчУГј°ЕRҙІ‘ӘУГғrЦө
- МХРgЙъОпјјРgЦvЧщоAёжЈәИЛ№ӨЦЗДЬЛҺОпФOУӢөДҢҚУГ·Ҫ·Ё
- КоЖЪёЈАы,ЗЪПиECL»ҜҢW°l№вТәФҮ„©ЎўәЛЛбИҫБПЩI¶юЛНТ»
- ГАөВВ•НЖіц·ЦЧУЙъОпҢWФ\”аҪвӣQ·Ҫ°ёЈ¬ә¬¶аҝоҷzңyФҮ„©
- ЙРоЈЙъОп618®aЖ·ДкЦРҙуҙЩ,ГвЩMФҮөИ»о„Ув »ЭҒнТu
- MCE”yКЦИA–|Һҹ·¶ҙуҢWҙтФмAIЛҺОпМҪЛчВ“әПҢҚтһКТ
- АвзRМ©ҝЛ19ҝоБчКҪФҮ„©«@ЧCЈ¬®aЖ·ҫШкҮ”UЦБ51ҝо
- ГАөВВ•НЖіц¶аҝо»щУЪРВТ»ҙъңyРтјјРgөДуwНвФ\”аФҮ„©әР
- Д¬ИрЙъОпVivoMatter»щЩ|Дz®aЖ·ФҮУГ»о„УЯMРРЦР