Claudin18.2的結構、功能基礎及其胃癌靶向藥物的研發現狀與挑戰
胃癌在癌癥相關死亡率中排名第三,被認為是全世界最難治愈的癌癥之一。在晚期或轉移性胃癌或胃食管交界處(GEJ)腺癌患者中,中位總生存期(mOS)不超過10個月。雖然人類表皮生長因子受體2(HER-2)靶向治療和免疫檢查點抑制劑已經為特定人群帶來福音,但在進展期胃癌中尋找其他靶點勢在必行,Claudin18.2(CLDN18.2)正是在這一背景下脫穎而出,成為極具潛力的胃癌治療新靶點。
Claudin18.2 的結構與功能基礎
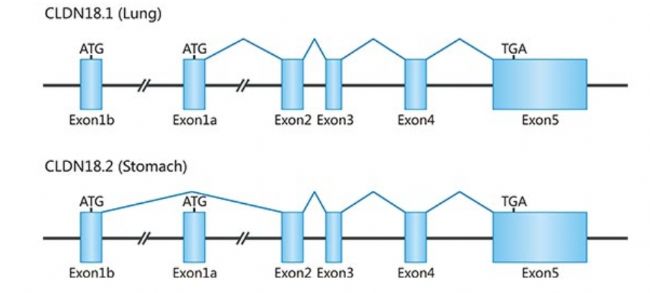
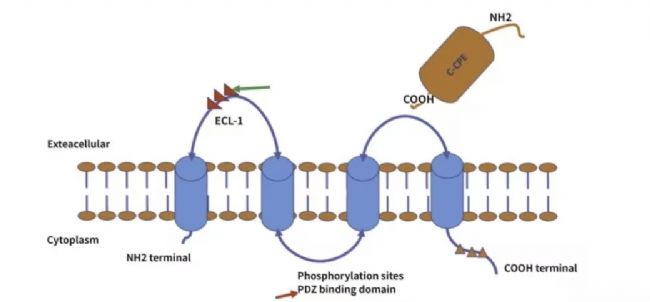
Claudin 家族作為緊密連接的重要組成部分,在維持細胞間分子交換的平衡和上皮細胞極性方面發揮著關鍵作用。Claudin 蛋白是四次跨膜蛋白,擁有獨特的結構,其細胞外環在形成緊密連接和發揮閘門功能中意義重大。而 CLDN18.2 作為 Claudin 家族中的胃特異性亞型,在正常生理狀態下,被保護于胃粘膜內,常規單克隆抗體難以接觸。但腫瘤發生時,癌細胞緊密連接受損,CLDN18.2 表位暴露,這一特性使其成為腫瘤靶向治療的理想靶點。此外,在胰腺癌、食管癌和肺癌等腫瘤中也發現了 CLDN18.2 的表達,進一步拓展了其在腫瘤治療領域的潛在應用范圍。
CLDN18.2 靶向藥物的研發現狀
目前,針對 CLDN18.2 的靶向治療藥物研發正如火如荼地進行。眾多藥企積極布局,多種類型的藥物處于不同研發階段。其中,Zolbetuximab 作為首款針對 CLDN18.2 的開發藥物,研究進展較為領先。從早期的人體臨床試驗到后續的多期研究,Zolbetuximab 在治療胃癌方面展現出了令人矚目的療效和安全性。在 IIa 期 MONO 2013 試驗中,它顯著延長了難治性晚期或轉移性 CLDN18.2 陽性胃腺癌患者的中位無進展生存期;在 IIb 期 FAST 2015 研究里,聯合 EOX 化療方案,不僅提高了客觀緩解率,還顯著延長了患者的總生存期。不過,Zolbetuximab 在臨床應用中也面臨一些問題,如不同試驗中的檢測手段和陽性閾值存在差異,這可能會影響對患者的篩選和治療效果評估。
除 Zolbetuximab 外,其他 CLDN18.2 靶向藥物也在不斷涌現。雙特異性抗體、ADC 藥物以及 CAR - T 細胞療法等都展現出了各自的優勢和潛力。像 AMG 910 這種 CD3/Claudin 18.2 雙特異性抗體,正在探索其在胃癌或胃食管交界處癌患者中的安全性和耐受性;CAR - T 細胞療法在 CLDN18.2 陽性實體瘤的治療中也取得了一定成果,部分患者達到了完全緩解或部分緩解。
CLDN18.2 靶向治療面臨的挑戰
CLDN18.2 靶向治療在臨床實踐中仍面臨諸多挑戰。檢測手段缺乏統一標準,不同檢測試劑可能導致陽性閾值和療效判斷的差異,這對于精準篩選患者和評估治療效果極為不利。CLDN18.2 作為預后評判指標的價值尚未完全明確,其與腫瘤分子亞型的關系存在爭議,且基因改變對其預后價值的影響也需要進一步探究。此外,目前對于 CLDN18.2 表達的最佳界限值尚無定論,不同試驗中的界限值差異可能會影響對患者的分層和治療決策。
聯合治療的探索與展望
聯合治療是 CLDN18.2 靶向治療的重要發展方向。理論上,靶向 CLDN18.2 可與化療、免疫治療、抗血管生成藥物等協同作用,提高治療效果。化療能增強 Zolbetuximab 誘導的 ADCC 效應,還可使腫瘤細胞對 Zolbetuximab 更敏感;免疫治療與 CLDN18.2 靶向治療聯合,有望促進 T 細胞浸潤和抗原遞呈,提升免疫檢查點抑制劑的療效。但在實際應用中,需要充分考慮不同人群對聯合治療的耐受性差異,尤其是東西方人群在藥物代謝和不良反應方面的不同表現。
CLDN18.2 作為胃癌靶向治療的新興靶點,為胃癌患者帶來了新的希望。雖然目前還存在一些問題和挑戰,但隨著研究的不斷深入、檢測技術的標準化以及聯合治療方案的優化,CLDN18.2 靶向治療有望在未來成為胃癌治療的重要手段,為改善胃癌患者的預后和生活質量做出重要貢獻。
產品信息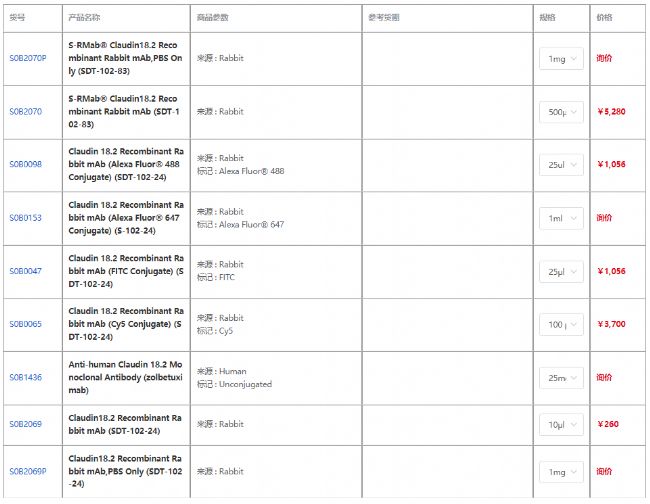
參考文獻
[1] Sahin U, TürECi Ö, Manikhas G, et al. FAST: a randomised phase II study of zolbetuximab (IMAB362) plus EOX versus EOX alone for first-line treatment of advanced CLAUDIN18.2-positive gastric and gastro-oesophageal adenocarcinoma [J]. Ann Oncol, 2021. 32(5): 609-619.
[2] Schneeberger EE, Lynch RD. The tight junction: a multifunctional complex [J]. Am J Physiol Cell Physiol. 2004, 286: C1213-28.
[3] Özlem Türeci; Michael Koslowski; Gerd Helftenbein, et al. Claudin-18 gene structure, regulation, and expression is evolutionary conserved in mammals [J]. Gene. 2011, 481(2), 83–92.
[4] Gunzel, D.; Yu, A. S. L. Claudins and the Modulation of Tight Junction Permeability [J]. Physiological Reviews. 2013, 93(2), 525–569.
[5] Klamp, T. et al. Highly specific auto-antibodies against claudin-18 isoform 2 induced by a chimeric HBcAg virus-like particle vaccine kill tumor cells and inhibit the growth of lung metastases [J]. Cancer Res. 2011, 71, 516-527.
[6] Sahin U, Koslowski M, Dhaene K, et al. Claudin-18 splice variant 2 is a pan-cancer target suitable for therapeutic antibody development [J]. Clin Cancer Res. 2008, 14: 7624–34.
杭州斯達特 (www.starter-bio.com)志在為全球生命科學行業提供優質的抗體、蛋白、試劑盒等產品及研發服務。依托多個開發平臺:重組兔單抗、重組鼠單抗、快速鼠單抗、重組蛋白開發平臺(E.coli,CHO,HEK293,InsectCells),已正式通過歐盟98/79/EC認證、ISO9001認證、ISO13485。