Nature:下一代減肥藥
來源:醫藥魔方Pro
減肥藥市場轟轟烈烈。2024年,兩大明星產品——減肥版司美格魯肽(Wegovy)和替爾泊肽(Zepbound)分別賣了84.48億美元(+86%)、49.26億美元(+270%),這無疑將進一步加劇減肥藥的研發熱潮。對于下一代減肥藥的開發,業界的目標是相比Wegovy、Zepbound提供更強大的減肥效果和更少的副作用。近日,Nature雜志發表了一篇專題報道,分析了即將問世的新一代減肥藥。
對于Kristian Cook來說,他打開的每一個披薩盒都是在減肥道路上關上的一扇門。在體重到達114 kg,且每天都需要服用治療高膽固醇、高血壓和痛風的藥物時,Cook決心采取行動。
2022年底,46歲的Cook參加了一項臨床試驗,該試驗旨在測試司美格魯肽(Wegovy)與一種有望在減少脂肪的同時保護肌肉的實驗性藥物(bimagrumab)的聯合療法。
肌肉損失是服用司美格魯肽(Wegovy)等減肥藥的人面臨的一個大問題。這些GLP-1R激動劑模擬一種天然的腸道激素——胰高血糖素樣肽1(GLP-1),以抑制食欲和調節代謝。然而,減少卡路里攝入會導致能量不足,身體通常會通過燃燒肌肉來彌補。Bimagrumab似乎可以抵消這種肌肉損失。
Bimagrumab是100多種處于不同開發階段的抗肥胖候選藥物之一。有可能在未來幾年獲批上市的下一波減肥藥與目前已上市的藥物類似。緊隨其后的是許多被開發用于同時實現“減重和肌肉保護”的療法。此外,還有幾十種藥物針對不同的生物學途徑,可能會在未來幾十年重新定義肥胖治療。
“我們正在努力創造下一代健康的減肥解決方案。” 在GLP-1藥物的早期開發中發揮了關鍵作用的Philip Larsen說道。Philip Larsen現在是瑞士一家專注于肥胖的初創公司SixPeaks Bio的首席執行官。
司美格魯肽和替爾泊肽的成功激發了減肥市場,但這兩種藥物都有局限性。它們需要每周注射一次,并經常引起令人不快的副作用,尤其是惡心、嘔吐和腹瀉。從長期來看,肌肉量的減少和停止治療后體重反彈的可能性也是問題。更重要的是,這些藥物對大約10%-30%的服用者不起作用。
新興療法旨在增強減肥效果,改善耐受性,確保長效療效,并為更廣泛的人群找到選擇。“我們將看到,不同的藥物對不同的人群更有效。” Weill Cornell Medicine的肥胖專家Louis Aronne說道。
 來源:Nature
來源:Nature不同的路線,相同的追求
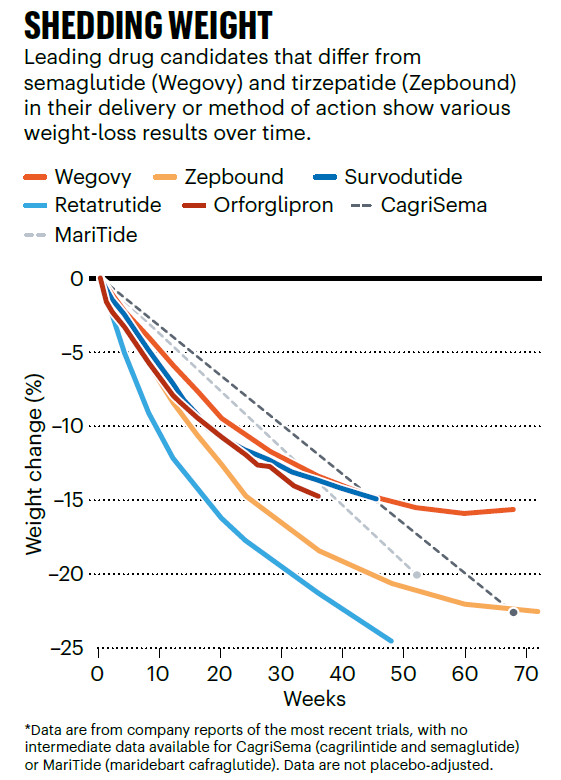
司美格魯肽和替爾泊肽是目前最熱門的GLP-1藥物,機制上來講,兩款藥物略有不同,前者只靶向GLP-1R,后者同時靶向葡萄糖依賴性促胰島素多肽受體(GIPR)。GIP進一步加速能量代謝,影響身體儲存和燃燒營養物質的方式。替爾泊肽的雙靶向機制被認為與其更優越的減肥效果有關。在一項由禮來發起的大型頭對頭試驗中,服用替爾泊肽的參與者平均減輕了20%的體重,超過了諾和諾德的司美格魯肽減重14%的效果。
受替爾泊肽的啟發,許多公司正在開發同時靶向GLP-1和GIP受體的雙激動劑藥物。根據醫藥魔方NextPharma®數據庫,截至目前,有20余款類似替爾泊肽的療法正在進行臨床試驗,如恒瑞醫藥/Kailera的HRS9531(III期臨床)、翰森制藥的HS-20094(III期臨床)、博瑞醫藥的BGM0504(III期臨床)等。
除了GLP-1R/ GIPR雙激動劑類藥物,也有公司正在開發激活GLP-1R但同時阻斷GIPR的雙靶向藥物,如安進的MariTide(II期臨床)。該公司發布的數據顯示,MariTide可以每月注射一次,52周平均減重20%。值得一提的是,MariTide顯示出在最后一次給藥后多個月內仍能維持減重。
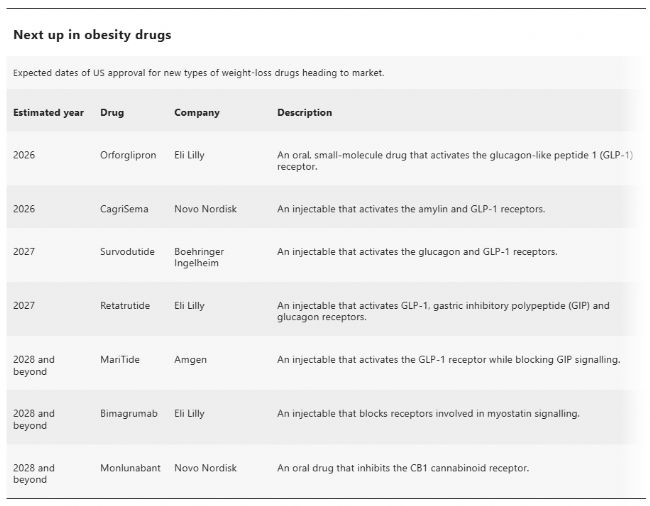
在給藥方面,業界在探索“每周注射一次”的替代方案。除了上文提到的每月注射一次,口服小分子GLP-1R激動劑也是值得關注的方向。禮來的orforglipron在嚙齒類動物身上顯示出與GLP-1注射液相似的結果。在一項為期36周的II期研究中,每天口服一次orforglipron的參與者體重減輕了15%。禮來預計將在2025年完成III期試驗,orforglipron可能在2026年獲得美國監管機構批準上市。
聯合的力量
除了基于GLP-1、GIP開發減肥藥物,一些制藥公司也在尋找其它激素靶點,其中包括其它腸道來源的激素,如肽YY(peptide YY,以能人有飽腹感而聞名),胰腺釋放的激素,如胰高血糖素(glucagon)、胰淀素(amylin),它們可以通過促進能量消耗、穩定血糖水平和進一步抑制食欲來補充GLP-1藥物。
目前在研的很多療法都是同時靶向多種途徑。例如聯合療法CagriSema(III期臨床)將長效的amylin類似物與司美格魯肽配對。諾和諾德表示,在為期68周的III期試驗中,參與者用這種療法平均減掉了近23%的體重。
如果正在進行的試驗取得成功,CagriSema以及BI的survodutide(GLP-1R激動劑&GCGR激動劑)最早可能在2026年或2027年獲得監管部門的批準。
不過,這些藥物的光芒可能會受到禮來另一款藥物retatrutide(III期臨床)的影響。Retatrutide同時靶向GLP-1, GIP 和胰高血糖素(glucagon)受體,在II期試驗中,48周平均減輕了24%的體重,為肥胖治療設定了新的基準。
來源:Nature
新靶點、老靶點
雖然腸道激素仍然是肥胖藥物開發的基石,但大規模基因測序已經成為新興靶點的靈感來源之一。2021年,Regeneron的科學家對近65萬人的DNA進行了分析,發現了一種與“低體重”有關的罕見基因變異,研究顯示,抑制 GPR75 可能是肥胖的一種治療策略,相關成果發表于Science雜志(推薦閱讀:“瘦子基因”找到了!再生元Science發文,揭示肥胖新靶點——GPR75)。
2022年,Alnylam的研究人員基于來自超36萬人的數據,確定了一種名為INHBE的基因突變與“腰臀比低”有關。INHBE編碼一種分泌蛋白——肝臟因子activin E。研究表明,activin E是腹部肥胖的潛在治療靶點。相關成果發表在Nature Communications雜志上。該公司目前正在試圖開發藥物,來重現這種基因突變的益處(推薦閱讀:燃燒我的卡路里!Alnylam發現“燃脂”新靶點)。
同時,一些“老靶點”也重新受到關注,例如大麻素受體CB1。2000年代末,基于該靶點的藥物rimonabant曾作為減肥療法在歐洲短暫銷售。但抑制大腦中的大麻素受體與一些人抑郁、焦慮和自殺念頭的風險增加有關。Rimonabant上市不到三年就退出了市場,競爭對手公司也放棄了類似的候選藥物。
不過,美國的神經內分泌學家George Kunos從未放棄過大麻素阻斷策略。大約15年前,他的團隊和其他研究人員在嚙齒動物身上證明,CB1抑制劑的大部分減肥功效來自肝臟、肌肉、胰腺和腦外其他器官的代謝途徑。如果像rimonabant這樣的藥物能夠經過化學修飾以防止其穿過血腦屏障,它可能會在不產生嚴重副作用的情況下帶來代謝益處。
Kunos的實驗室開發了這樣一種新一代CB1靶向藥物——monlunabant(CB1反向激動劑),現由諾和諾德研發。盡管去年的II期試驗結果表明,monlunabant仍然會引起焦慮、易怒和睡眠障礙,但Kunos預測,諾和諾德能夠達到一種劑量,既能顯著減輕體重,副作用又在可接受的水平上。
肌肉“守衛戰”
以bimagrumab為代表的肌肉導向療法(muscle-directed therapies)也引起了業界的極大興趣。這在很大程度上是因為服用司美格魯肽和替爾泊肽的個體中,大約三分之一的體重減輕來自肌肉的減少,而不是脂肪的減少。
肌肉量的減少會引起美容方面的擔憂,并會降低力量、靈活性和整體生理健康。肌肉在葡萄糖調節和能量消耗中也起著至關重要的作用。“因此,肌肉損失是可持續減肥的主要障礙。” 馬薩諸塞州總醫院研究bimagrumab的內分泌學家Melanie Haines說道。
Bimagrumab通過阻斷一種受體發揮作用,基于該受體,肌肉生長抑制素和相關蛋白抑制肌肉生長,促進脂肪保留。在接受bimagrumab聯合司美格魯肽治療近一年后,Cook減掉了近18 kg的脂肪,同時增加了1kg的肌肉。不良反應方面,Cook稱主要是偶爾會抽筋和痙攣。
現在,Cook已經完全停止了藥物治療,他的脂肪又增加了一些。但他的體重仍比巔峰時期低10%以上,肌肉量也保持相對穩定。“對我來說,這是一次改變人生的經歷。” Cook說道。
一些其他公司也在開發肌肉導向療法,如制藥公司Veru正在開發一款口服藥物enobosarm(聯合Wegovy)。參與了bimagrumab和其它減肥藥試驗的肥胖專家Steven Heymsfield希望,肌肉導向療法可以成為治療肥胖的豐富藥物選擇的一部分。
Regeneron也在開發肌肉導向療法,公司高級副總裁兼內科臨床開發部門負責人Boaz Hirshberg認為,司美格魯肽和替爾泊肽不會單獨存在太久。“隨著其它治療選擇的出現,可以考慮如何根據患者的需求定制治療方案。”他說。