øČž°ûÖÎŊŪaIÓíÐÂrīú
ž°ûÖÎŊĘĮÖļĀûÓÃÄģÐĐūßÓÐĖØķĻđĶÄÜĩÄž°ûĩÄĖØÐÔĢŽēÉÓÃÉúÎïđĪģĖ·―·ĻŦ@ČĄšÍ/ŧōÍĻß^ówÍâUÔöĄĒĖØĘâÅāðBĩČĖĀíšóĢŽĘđß@ÐĐž°ûūßÓÐÔöÃâŌߥĒĒËĀēĄÔówšÍÄ[Áöž°ûĄĒīŲßM―MŋÆũđŲÔŲÉúšÍCówŋĩÍĩČÖÎŊđĶЧĢŽÄķøß_ĩ―ÖÎŊžēēĄĩÄÄŋĩÄĄĢž°ûÖÎŊžžÐgÄąūŲ|ÉÏé°Đ°YĩČÖØëUžēēĄĖáđĐÁËČŦÐÂĩÄ―âQ·―°ļĢŽŌēģÉéÅcËĀÍöēŦķ·ĩÄēŧÐŌŧžÕßĩÄŲFÏĢÍûĄĢ2013ÄęĢŽž°ûÖÎŊžžÐgļüąŧĄķŋÆWÞDŧŊátWĄ·ësÖūÔuéÄęķČĘŪīóŋÆžžÍŧÆÆÖŪĘŨĄĢž°ûÖÎŊ°īÕÕž°û·NîŋÉŌÔ·ÖéļÉž°ûÖÎŊšÍÃâŌßž°ûÖÎŊĄĢ
ļÉž°ûÖÎŊĘĮÖļĀûÓÃŨÔówŧōÕßŪówđĮËčŧōħÔėŅŠļÉž°ûŌÆÖēÖÎŊŅŠŌšēĄšÍšÐÔÄ[ÁöĢŽŧōĀûÓÃđĮËčšÍħĩČíÔīĩÄégģäŲ|ļÉž°û―ŌÆÖēšóÞDŧŊéģÉđĮž°ûĄĒÐÄžĄž°ûĩČÓÃÓÚÖÎŊĄĢļÉž°ûÖÎŊÉæž°ÖÎŊĩÄžēēĄąČÝ^V·šĢŽÓÖŋÉŌÔž·ÖéģÉówļÉž°ûĢÛÔėŅŠļÉž°û(HSC)ĢĶégģäŲ|ļÉž°û(MSCs)ĢÝĄĒÅßĖĨļÉž°û(ESC)šÍÕT§ķāÄÜļÉž°û(iPSC)ĄĢ
ÃâŌßž°ûÖÎŊÓÖ·Qž°ûß^Ā^ÃâŌßÖÎŊĢŽĘĮĒŧžÕßÃâŌßž°û―ówÍâĖĀíĢŽžÓČëĖØŪÐÔŋđԚ͞°ûŌōŨÓīĖžĪĢŽšYßxēĒīóÁŋUÔöūßÓÐļßķČĖØŪÐÔĩÄÃâŌßЧŠž°ûĢŽČŧšóŧØÝĩ―ŧžÕßówČĒįÄ[Áöž°ûŧōēĄķūĢŽÔÚÅRīēŠÓÃrķāŌÔŨÔówÃâŌßž°ûéÖũĄĢÖũŌŠáĶÄ[Áöž°ÃâŌßÏāęPÐÔžēēĄĢŽ°īÕÕŋđÔĖØŪÐÔÓÖŋÉŌÔž·Öé·ĮŋđÔĖØŪÐÔÃâŌßž°ûÖÎŊšÍŋđÔĖØŪÐÔÃâŌßž°ûÖÎŊĄĢĮ°Õß°üĀĻĢšž°ûŌōŨÓÕT§ĩÄĒûž°ûĢĻCIKĢĐŊ·ĻĄĒäÍŧ îž°ûĢĻDCĢĐŊ·ĻĄĒDC īĖžĪĩÄ CIK ž°ûDC- CIK ž°ûŊ·ĻĄĒŨÔČŧĒûž°û(NK)Ŋ·ĻšÍŌÔäÍŧ îž°û(Dendritic cells, DCs)éŧųĩAĩÄž°ûķūÐÔTÁÜ°Íž°ûĢĻcytotoxic T lymphocyte,CTL)Ŋ·ĻĄĒÄ[Áö―þÐÔÁÜ°Íž°ûĢĻtumor infiltrating lymphocyte cellsĢŽTILĢĐĄĒž°ûķūÐÔ T ž°ûĢĻcytotoxic T-lymphocyteĢŽCTLĢĐĄĒĶÃĶÄT ž°ûšÍÁÜ°ÍŌōŨÓŧîŧŊĩÄĒûž°ûĢĻLAK ž°ûĢĐĢŧšóÕß°üĀĻTž°ûĘÜów(T cell receptorĢŽTCR)ŧųŌōÐÞïTž°û(TCRĄŠT)šÍĮķšÏŋđÔĘÜów(chimetric antigen receptorĢŽCAR)ÐÞïTž°û(CARĄŠT)ĄĢ
ž°ûÖÎŊ―üÄęíĘĮÖÐÍâŅÐūŋÕßęPŨĒĩÄáéTÔî}ĢŽđPÕßŌÔĄ°ž°ûÖÎŊĄąéęPæIŨÖÔÚ web of sciencezËũŨî―ü10Äę°ląíĩÄŅÐūŋģÉđûĢŽ―Yđû°lŽF2008ÄęŌÔšóęPÓÚž°ûÖÎŊîIÓōĩÄÕÎÄšÍĩÁŋÖðÄęßfÔöĢŽÖąÖÁ―üÉÄęÔîIÓōĩÄÏāęPÕÎÄšÍĩÁŋēÅÉÔÓÐÏÂ―ĩĢŽĩŦÔÚ2017ÄęŋĩÁŋŌĀČŧļßß_136138ÆŠĄĢ
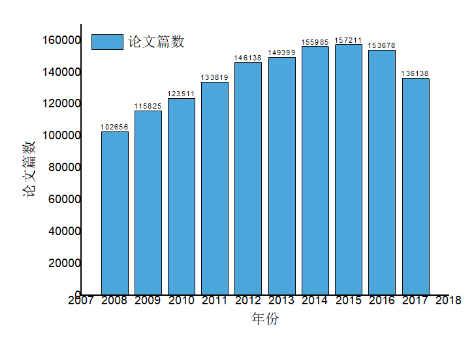
―ß^ķāÄę°lÕđĢŽÎŌøļÉž°ûŅÐūŋŌŅ―ÔÚž°ûÖØūģĖĄĒķāÄÜÐÔÕ{ŋØĄĒßzũšYßxšÍÐÞïĄĒĖØÉŦÓÎïŲYÔīÆ―Å_ĩČ·―ÃæĖÓÚøëHîIÏČËŪÆ―ĢŽēŋ·ÖŅÐūŋCšÍŋÆŅÐČËTĩÄøëHÓ°íï@ÖøĖáÉýĄĢĀýČįÖÐŋÆÔšVÖÝÉúÎïátËÅc―ĄŋĩŅÐūŋÔšÅáķËĮäÔšéLÔÚÔŲÉúátWîIÓōČĄĩÃÁËķāíūßÓÐÖØīóÓ°íÁĶĩÄ°lŽFĢŽÔÚČŦĘĀ―į·ķúČĢŽĘĮÔîIÓōĩÄŌŧÎŧŌýîIÕߥĢļÉž°ûÖÎŊŪaIĩÄ°lÕđëxēŧé_ŪaWŅÐĩÄūCšÏŌŧówÍÆÓĄĢÄŋĮ°ĢŽøČĘÐöÓÐķāžŌCđēÍŽ°lÁĶĢŽéÍÆßMÎŌøļÉž°ûžžÐgĩÄÞDŧŊÂäĩØĢŽøČîIÏČÆóIŌŅ―ÅcátÔšĄĒŋÆŅÐCĩČÕđé_īóÁŋĩÄšÏŨũĄĢĀýČįĢŽēĐŅÅŋØđÉžŊFÍĻß^
ĮëAÆ―átWŧų―ðþÅc―ü40ÓāžŌátÔššÏŨũĢŽé_ÕđĖĨąPļÉž°ûÖÎŊŨÔówÃâŌßžēēĄĄĒđĮęPđŅŨĄĒĩØÖКĢØŅŠĄĒÔįËĨ°YĩČžēēĄĩÄÅRīēŅÐūŋĢŽđēÍŽÍÆßMĖĨąPļÉž°ûÄŧųĩAŋÆŅÐĩ―ÅRīēŠÓÃĩÄŋėËŲÞDŧŊĄĢÔÚīæĶž°ŪaIŧŊé_°l·―ÃæĢŽÎŌøĘÐöÉÏŌēŌŅ―ÓŋŽFģöŌŧÅúŠūßĖØÉŦĩÄÆóIĢŽČįÐÂÉúÃüĄĒÖÐÔī
fšÍĄĒąąŋÆÉúÎïĩČĄĢ
ÎŌøĩÄÃâŌßž°ûÖÎŊŅаlĮ°ÆÚķāžŊÖÐÔÚ·ĮĖØŪÐÔÃâŌßž°ûŊ·ĻĢŽĩŦß@ŨÄęŌÔCAR-TžžÐgéīúąíĩÄĖØŪÐÔÄ[ÁöÃâŌßž°ûÖÎŊ°lÕđŅļËŲēĒČĄĩÃÁËōČËģÉŋĄĢÆäÖÐËđĩĪŲđŦËūŌŅÍęģÉÁË26 ĀýŧžÕßĩÄCAR-T ÖÎŊšÍģõē―ĩþĘÕžŊĢŽÆäÖÐ23 ÃûŧžÕßß_ĩ―ÁËÍęČŦū―âĢŽÍęČŦū―âÂĘß_88.5%ĢŽÔōĩþ―Ó―üÃĀøÍŽÐÐĩÄŅÐūŋģÉđûĢŽžžÐgÅcÃĀøÍŽē―ĢŽēĒŌŅ―îIÏČÓÚWÖÞšÍČÕąūĩČÆäËûøžŌšÍĩØ ^ĄĢÎũąČÂüÉúÎïŋÆžžĢĻÉÏšĢĢĐÓÐÏÞđŦËūĩÄCAR-T ÅRīēŅÐūŋÖũŌŠÅc―â·ÅÜ301 átÔšíné|―ĖĘÚšÏŨũĢŽÔÚŅŠŌšÄ[ÁöšÍķā·NîÐÍówÁöÉÏČĄĩÃÁËŠīðĢŽŅаlßMķČĖÓÚøëHîIÏČĄĢ
ž°ûÖÎŊŪaIÔÚÎŌøĩÄ°lÕđŋÉÖ^Ũ―ēĻÕÛĢŽ2012ÄęÐlÉúēŋ―ÐÍĢÁËÔÚÖÎŊšÍÅRīēÔōÖÐĘđÓÃČΚÎÎī―ÅúĘĘđÓÃĩÄļÉž°ûĢŽēĒÍĢÖđ―ÓĘÜÐÂĩÄļÉž°ûíÄŋÉęÕĄĢ2016ÄęĩÄĄ°ÎštÎũĘžþĄąŨÕýÔÚÆDŋāĖ―ËũĮ°ßMĩÄÃâŌßž°ûŊ·ĻKÔâÐÅČÎÎĢCĄĢķøÔÚß^ČĨĩÄ2017ÄęŋÉÖ^ĘĮž°ûÖÎŊĩÄŌŧīóÄęĢŽÆÚÅÎŌŅūÃĩÄÖļ§ÕþēߥĒÏāęPŌ·ķšÍËĘÏāĀ^ąŧÍÆģöĄĢ
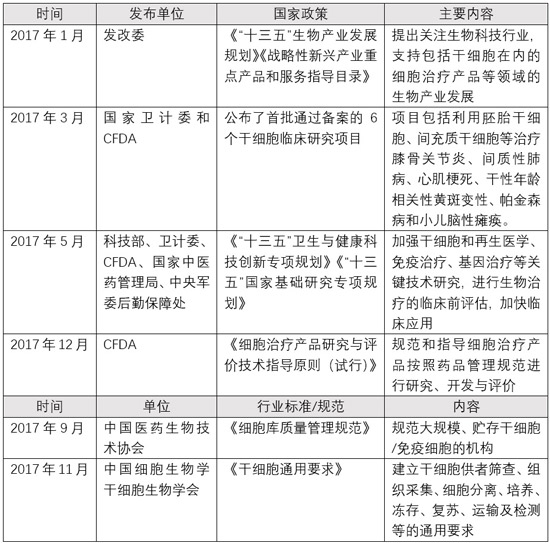
2017ÄęÃâŌßž°ûÖÎŊŌēÓíÖØīóÍŧÆÆĢŽ8ÔÂ30ČÕĢŽFDAÅúĘÖZČAĩÄCAR-TŊ·ĻCTL019ÉÏĘÐĢŽÓÃÓÚÖÎŊÍ°lŧōëyÖÎÐÔšÍŊšÍÄęÝpģÉČËBž°ûžąÐÔÁÜ°Íž°û°ŨŅŠēĄĢŧ2017Äę10ÔÂ18ČÕĢŽÃĀøFDAÕýĘ―ÅúĘÁËČŦĮōĩÚķþCAR-TŊ·ĻĢŽíŨÔKiteĩÄKTE-C19ÉÏĘÐĢŽÓÃÓÚÖÎŊÍ°lŧōëyÖÎÐÔīóBž°ûÁÜ°ÍÁöĩÄģÉČËŧžÕߥĢëSÖøĄķž°ûÖÎŊŪaÆ·ŅÐūŋÅcÔuržžÐgÖļ§ÔtĢĻÔÐÐĢĐĄ·ĩÄÂäĩØĢŽÎŌøĩÄķāžŌCšÍÆóIé_ÕđÁËCAR-TŪaÆ·ĩÄÅRīēÉęóđĪŨũĄĢ―ØÖđ2018Äę2ÔÂ9ČÕĢŽøČŌŅÓÐ9CAR-Tž°ûËÎïĩÄ10íINDÉęÕąŧCDEģÐÞkĘÜĀíĢŽÆäÖÐÄÏūĐũÆæĘĮÄÃĩ―CAR-Tž°ûÖÎŊÅRīēÅúžþĩÄđŦËūĢĻČįÏÂDĢĐĄĢ
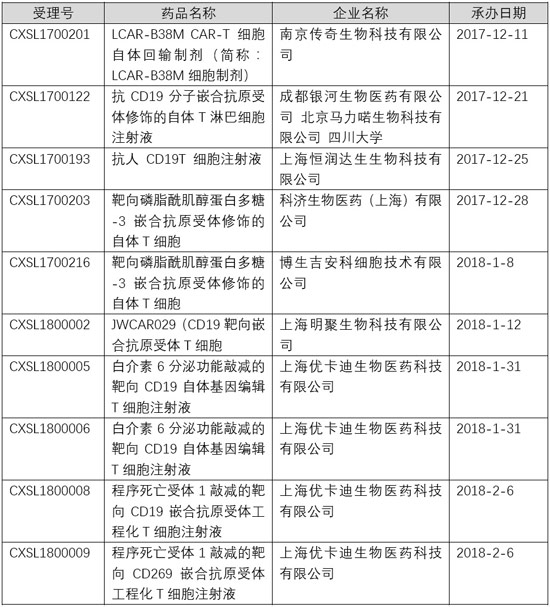
ÐÅÏĒíÔīÓÚCFDAūWÕū
2017ÄęĢŽĘĮÎŌøž°ûÖÎŊŪaIĀûšÃÕþēßĩÄūŪÄęĄĢČį―ņ2018ÄęēÅĀé_áĄÄŧĢŽž°ûÖÎŊîIÓōąãũíÁËŌŧÓÖŌŧĩÄšÃÏûÏĒĄĢøžŌÐlÓÎŊ―üČÕŋŊģöęPÓÚÕþ
fÎŊTĢšĄ°ļÄßMļÉž°ûÅRīēŅÐūŋĘČëËĘĄąĖá°ļĩÄīðÍšŊĄĢīðÍÖÐÃũī_ÖļģöĢš―ņšóĢŽëSÖøļÉž°ûîIÓōŅÐūŋđĪŨũĩÄēŧāÉîČëĢŽđÜĀíówÖÆCÖÆēŧā―ĄČŦĢŽøžŌÐlÉúÓÉúÎŊšÍĘģÆ·ËÆ·ąOđÜŋūÖĒßmrĶĄķļÉž°ûÅRīēŅÐūŋđÜĀíÞk·ĻĢĻÔÐÐĢĐĄ·ßMÐÐÐÞÓÍęÉÆĢŽŌÔßmŠÎŌøļÉž°ûÅRīēŅÐūŋĩÄ°lÕđ îršÍđÜĀíÐčĮóĄĢøžŌÖŠŨRŪaāūÖ°lēžĩÄ2018ÄęаæĄķÖŠŨRŪaāÖØücÖ§ģÖŪaIÄŋ䥷ĢŽÃũī_ĒļÉž°ûĄĒÃâŌßž°ûÖÎŊĩČühÖÐŅëĄĒøÕÔšÎÄžþÃũī_ĩÄÖØüc°lÕđ·―ÏōÁÐéÖØücÖ§ģÖŪaIĄĢß@ŌâÎķÖøÎŌøļßķČÖØŌļÉž°ûÖÎŊĢŽļũíÖ§ģÖÕþēß―oļÉž°ûÖÎŊĖáđĐÁËÁžšÃĩÄ°lÕđhūģĄĢ
ž°ûÖÎŊÐÐIĘĮŌŧĄ°åXĄąū°VéĩÄÐÐIĄĢļųþČŦĮōĘÐöĮéóC Infiniti Research°lēžĩÄĩþĢŽ2017ÄęÖÁ2022ÄęÖŪégĢŽČŦĮōļÉž°ûÖÎŊĘÐöĒŌÔ36.52%ĩÄÍšÏÄęÔöéLÂĘÔöéLĄĢ2018ÄęĢŽČŦĮōļÉž°ûátŊĘÐöîAÓĒģŽß^Į§|ÃĀÔŠĄĢļũīóŅÐūŋCÅcÆóIŌēŋīĘÁËrCĢŽé_Õđž°ûÖÎŊŪaÆ·ŅаlÖÆäĩÄÉîķČšÏŨũĄĢĀýČįĢŽ2018Äę1ÔÂ19ČÕĢŽGE átŊÐûēžÅcÎũąČÂüÉúÎïŋÆžžžŊFšĘðēÉŲŌâÏōøĢŽšóÕßĩÄÉÏšĢđĪSĒĘđÓÃGEátŊĩÄž°ûÖÎŊė`ŧîÉúŪaÆ―Å_žžÐgĢŽŌÔžÓËŲÎũąČÂüÔÚž°ûÖÎŊîIÓōĩÄÐÂÉúÎïËÅRīēÔōž°ÉĖIŧŊßMģĖĄĢšĢÄÏšĢËŌēÔÚÍŽÔÂ21ČÕÍíégđŦļæĢŽđŦËūČŦŲYŨÓđŦËūšĢËÍķŲYÅcÉÏšĢŋĻĩÏÉúÎïátËŋÆžžÓÐÏÞđŦËūšĘðÁËðÂÔšÏŨũŋōžÜ
fŨhĢŽŋĻĩÏÅcšĢËÍķŲYĒúĀ@ÉúÎïát˚͞°ûÖÎŊîIÓōé_ÕđšÏŨũĢŽëp·―ÓÔÚšĢÄÏēĐöšÏŨũ―ĻÁĒŧųŌōÅcž°ûÖÎŊÖÐÐÄĄĢ
ūÍÄŋĮ°ĩÄĮéríŋīĢŽÉÏšĢĄĒąąūĐĄĒÉîÛÚĄĒVÖÝĘĮÎŌøž°ûÖÎŊŪaWŅÐÝ^éŧîÜSĩÄ ^ÓōĢŽÏČšó°lēžÕþēßžÓËŲÍÆÓÁËļÉž°ûžžÐgšÍŪaÆ·ĩÄÅRīēŠÓÚÍÅúĄĢÔįÔÚ2016ÄęĢŽÉîÛÚūÍ°lēžÁËĘŨž°ûÖÆäÖÐÐÄ―ĻÔOĩØ·―ËĘĄķž°ûÖÆäÖÐÐÄ―ĻÔOÅcđÜĀíŌ·ķĄ·ĢŽéÁËÍÆßMž°ûÖÆäž°·þÕĩÄËĘŧŊĢŽÔËĘžŧŊĩ―ÁËž°ûÅāðBĩÄķþŅõŧŊĖžÅāðBÏäĩÄįūúđĶÄÜÖļ§Ō·ķé90Ąæņáįūúß@ÓĩÄžđĄĢīËÍâĢŽÎũÄÏĄĒ|ąąĄĒšÓÄÏĩČĩØŌēÓÐÖTķāļßūŦžâČËēÅĄĒîIÏČCšÍÆóIÔÚēŧāÍÆÓÔĩØ ^ž°ûÖÎŊÐÐIĩÄēŧā°lÕđĄĢ
2017ÄęøČž°ûÖÎŊŪaIŌŅ―ÖØÕûÆėđÄP·ŦÆðš―ĢŽĮ°·―žČģäMCÓöÓÖģäMĖôðĄĢÏāÐÅ2018ÄęëSÖøÔîIÓōžžÐgĩÄēŧāÍŧÆÆĄĒÉĖIŧŊßMģĖĩÄČÕŌæĖáËŲĢŽž°ûÖÎŊŪaIĒÓíŲÓÚŨÔžšĩÄÐÂrīúĢĄ
ĒŋžÎÄŦI
[1]ķÖūÂĄ,ĒŅó,ÓČ,ĩČ.ž°ûÖÎŊîIÓōÐÂßMÕđ[J].ÖÐøÅRīēátÉúësÖū,2017,45(7):7-8.
[2]ÍõŽ,ęūwšį,ÓÚŋĄý,ĩČ.ž°ûšÍŧųŌōÉúÎïÖÎŊîIÓōÕđÍû[J]. ÉúÎïŪaIžžÐg,2017,2:2-84.
[3]ÆæÎÄ. GE átŊÖúÁĶÎũąČÂüžÓËŲž°ûÖÎŊËÎïÉúŪa[N]. ÖÐøátËó,2017,7.
[4]Ë{ïw.ļÉž°ûËĘŧŊ―ĻÔOÔŲßMŌŧē―[N]. átË―úó,2018,12.
[5]ÓášĢēĻ,ÖÜÖĮV. ž°ûÃâŌßÖÎŊĩÄŅÐūŋßMÕđž°ŠÓÃ[J]. ÖÐøátësÖū,2017,19(1):1-3.
- Ōŧ·Nž°ûÍâÄŌÅÝÍĻÓÃËÓ·―·ĻÖŪūÛĖĮå^ķĻÉđâËÓēßÂÔĩÄŅÐūŋÅc―é―B
- ž°ûÍâÄŌÅÝÔÚŌšówŧîzÖÐÅRīēŠÓÃđēŨR―âŨx,EVsÄōĘŌĩ―ēĄīēß ĩÄŋįÔ―
- ÖŽëÄ―é§CRISPR-Cas9ßfËÍŧųŌōūÝÔÚßzũÐÔŅÛēĄÖÎŊз―·ĻÖÐĩÄŠÓÃ
- ApogeeFlowž{ÃŨÁũĘ―xÖúÁĶÎĒÉúÎïzyžžÐgļïÐÂ
- CDEÎÄÕÂ―âŨxĢšîA·ĀÓà mRNA ŌßÃįÖŽŲ|ž{ÃŨîwÁĢŲ|ÁŋŅÐūŋ
- ApogeeFlowž{ÃŨÁũĘ―yĘÖ÷WÔ\ËųÍÆÓž°ûÍâÄŌÅÝĢĻEVĢĐ·ÖÎöÐÂÍŧÆÆ
- ÎÄŦI―âŨxĢšž°ûÍâÄŌÅÝšÍÖŽŲ|ž{ÃŨîwÁĢĩÄlÐÎīaës―ŧÖúÁĶËÎï°ÐÏōßfËÍ
- ž{ÃŨÁũĘ―zyžžÐg (nFCM) ÔuđĀÁų·NÄĪČžÁÏËÓž°ûÍâÄŌÅÝĩÄÐÔÄÜŅÐūŋ
- ßMŋÆņY°ēŋÆžžŅûÄú ĒžÓ2025 ĢĻÉîÛÚĢĐž°ûÍâÄŌÅÝīóþ
- ļĢÁũÖąēĨîAļæĢšČįšÎÓÃηÖŨÓÁũĘ―žžÐgzyž{ÃŨîwÁĢĢŋ
- ßMŋÆņY°ēyÁũĘ―·ÖÎö·ÖßxxĩČ ĒžÓ2025ÖÐøÄcĩĀīóþ
- EMA°lēžÐ°æmRNAŌßÃįŲ|ÁŋÖļÄÏēÝ°ļĢŽNanoFCMÖúÁĶzy
- ĀâįRĖĐŋËøŪaÁũĘ―ž°ûxĘŨīΰlØšĢÍâĘÐöŨßÏōĘĀ―į
- ÉîķČĶÔØŋËÂüė ĖØÉúÃüŋÆWÖÐø ^ŋ―ĀíÖÜĨ
- NanoFCMŅûÄú ĒžÓøëHž°ûÍâÄŌÅÝīóþISEV2025
- ÏēÓĢšĀâįRĖĐŋËÁũĘ―ž°ûxŦ@CEÕJŨCĢĄßMÜøëHĘÐö