賽業生物OX40人源化小鼠,助力腫瘤研究

想獲得國自然選題思路,提高國自然基金申請命中率?想調整研究方向,獲得學術研究突破口?有機會發高分文章?你需要了解學科發展態勢和未來走向!賽業生物專欄《Gene of the Week》每周會根據熱點研究領域介紹一個基因,詳細為您介紹基因基本信息、研究概況和應用背景等,助您保持學術研究敏銳度,提高科學研究效率,期待您的持續關注哦。今天我們要講的主角是下一代免疫治療靶點OX40。
免疫檢查點是指免疫細胞擁有的一組具有調節和控制免疫應答持久性同時保持自我耐受的信號通路分子。免疫檢查點可以是刺激性或抑制性的。免疫應答的功效由共刺激信號和共抑制信號之間的微妙平衡決定。抗原性的MHC/肽復合物與T細胞受體相互作用誘導的信號傳導是T細胞活化的先決條件,但不足以單獨啟動T細胞反應。共刺激分子的進一步信號傳導對于T細胞的最佳啟動、擴增和分化至關重要。這些分子主要分為兩大類:免疫球蛋白超家族(IgSF)和腫瘤壞死因子受體超家族(TNFRSF)。OX40是腫瘤壞死因子受體超家族成員4(TNFRSF4),是一類重要的T細胞共刺激分子,曾被人喻為繼PD-1/L1之后的又一藍海。
OX40(CD134)是一種1型跨膜糖蛋白,OX40L是OX40的配體,它們在活化的CD4,CD8 T細胞以及其他幾種淋巴和非淋巴細胞上表達,調節T細胞,抗原呈遞細胞和自然殺傷(NK)細胞產生的細胞因子,并調節細胞因子受體的信號傳導。
OX40可以誘導抗凋亡(Bcl-2、Bcl-xl和Bfl-1)和細胞周期(Survivin)蛋白的表達。OX40可抵消免疫細胞(包括CD4+和CD8+T淋巴細胞、NK細胞和B淋巴細胞)的抑制,同時直接刺激效應T細胞。
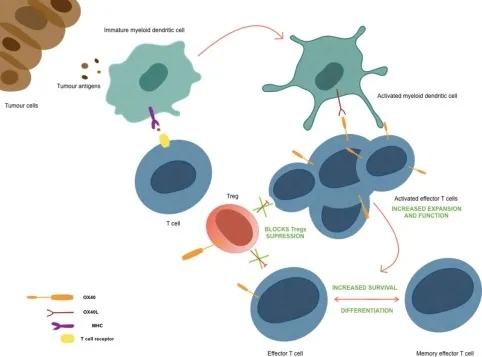
圖1. OX40的作用機制
對于抗CTLA-4治療,有證據表明通過表達Fcγ受體的巨噬細胞選擇性清除TME中的Treg細胞,這表明OX40定向抗體也可以消耗TME中的OX40+ Treg,而不會減少表達該受體的效應T細胞。Zhang等人表明,OX40共刺激導致FOXP3基因表達的抑制,這對Treg分化至關重要,這是通過兩個獨立的機制:增強激活蛋白1轉錄因子BATF、BATF3的表達以及激活AKT-雷帕霉素的哺乳動物靶標(mTOR)途徑。在臨床前模型中,有證據表明,抗OX40單克隆抗體(mAb)處理后,腫瘤浸潤的Treg細胞可降低IL-10的產生,從而使樹突狀細胞(DC)成熟,這可能是由于下調了轉錄因子干擾素調節因子1 mRNA的表達。因此,它產生了一種允許的免疫狀態,并導致髓樣細胞的積累以及先天性和適應性免疫的發展,這是抗OX40的抗腫瘤作用的重要步驟。
考慮到使用共刺激受體作為靶向治療以增強針對腫瘤的免疫反應的生物學原理,并且基于體外結果,已經開發了許多刺激OX40信號傳導的藥物:OX40特異性激動劑抗體、OX40L-Fc融合蛋白、用OX40L mRNA轉染DC以及工程改造為在表面表達OX40L的腫瘤細胞。
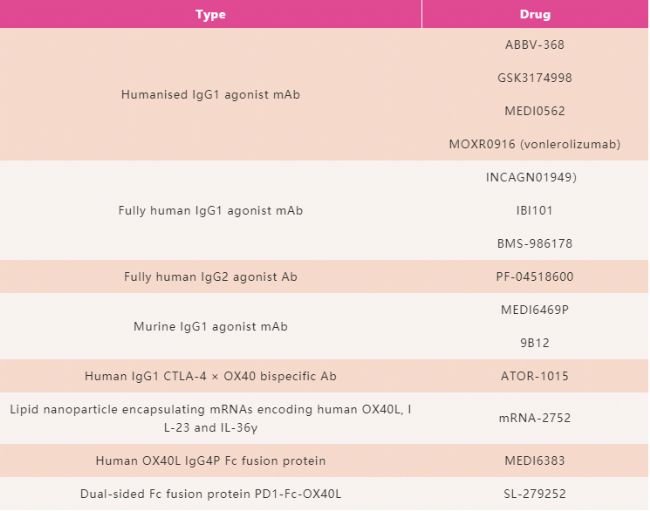
表1. 靶向OX40的藥物
在幾種臨床前癌癥模型中已顯示出針對OX40的免疫細胞調節和抗腫瘤活性,抗OX40和抗CTLA-4的聯合治療導致CD4+和CD8+T細胞的增殖和活性顯著增加,與抗OX40單藥治療相比,轉化為更好的結果。雖然OX40靶向治療在荷瘤小鼠身上顯示了令人印象深刻的結果,但初步的臨床數據表明,其作為單一療法在人類中的療效并不高。OX40共刺激與針對抑制性受體如抗PD-1和抗PD-L1的免疫療法結合使用是一種很有前途的策略。期待聯合療法能夠早日在臨床研究中得到驗證,為更多患者帶來創新療法。
參考文獻:
1. Silva C A C, Facchinetti F, Routy B, et al. New pathways in immune stimulation: targeting OX40[J]. ESMO Open, 2020, 5(1).
2. Webb G J, Hirschfield G M, Lane P J L. OX40, OX40L and Autoimmunity: a Comprehensive Review[J]. Clinical Reviews in Allergy & Immunology, 2016, 50(3):312-332.
賽業生物OX40人源化小鼠,助力腫瘤研究
品系背景:C57BL/6N
品系構建策略:
在小鼠OX40基因位點敲入人源OX40構建而成,該人源化模型表達了一個全人源化的OX40蛋白,包括人源胞外、跨膜和胞內結構域。
品系說明:
■ hOX40在小鼠體內表達具有正常的生理表達和調節模式。
■ 保留了靶點和配體的相互作用。
■ 小鼠的免疫系統功能健全。
■ 缺乏小鼠靶基因的表達,從而避免了交叉反應。
研究應用:
能在免疫系統功能健全的小鼠中進行靶向人免疫檢查點OX40的免疫腫瘤藥物的體內功效評估和分析。
模型驗證:
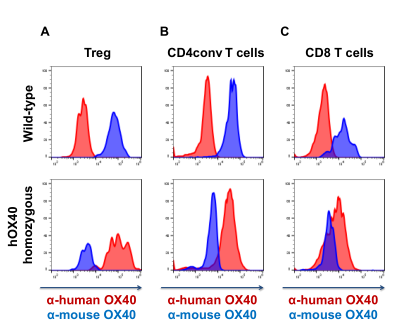
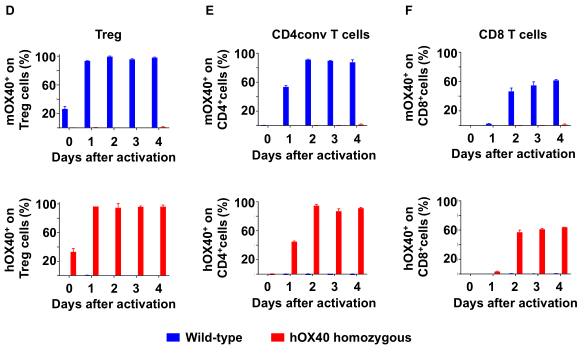 圖2. hOX40表達模式與mOX40在野生型小鼠的表達模式一致。在mIL-2的存在的前提下,用αCD3 /αCD28激活脾細胞、hOX40和 mOX4分別在hOX40小鼠和野生型小鼠的(A)Tregs亞群(viable,CD3+CD4+CD25+Foxp3+)、(B)CD4+ (viable,CD3+CD4+Foxp3+) 和(C)CD8+(CD3+CD8+)T細胞上分別表達。hOX40和mOX40在hOX40小鼠和野生型小鼠的(D)Treg、(E)傳統CD4和(F)CD8 T細胞上的表達動力學。
圖2. hOX40表達模式與mOX40在野生型小鼠的表達模式一致。在mIL-2的存在的前提下,用αCD3 /αCD28激活脾細胞、hOX40和 mOX4分別在hOX40小鼠和野生型小鼠的(A)Tregs亞群(viable,CD3+CD4+CD25+Foxp3+)、(B)CD4+ (viable,CD3+CD4+Foxp3+) 和(C)CD8+(CD3+CD8+)T細胞上分別表達。hOX40和mOX40在hOX40小鼠和野生型小鼠的(D)Treg、(E)傳統CD4和(F)CD8 T細胞上的表達動力學。
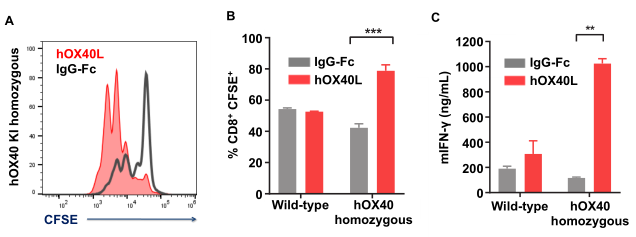
圖3. hOX40在體外對效應T細胞起作用。αCD3/αCD28激活從脾臟和淋巴結分離的T細胞(CD8+T細胞),hOX40L或IgG-Fc處理CD8+T細胞,可以看到hOX40L處理下,明顯促進了人源化OX40小鼠的CD8+T細胞的增殖和IFNγ的分泌。(A)流式圖;(B)代表性直方圖;(C)ELISA檢測培養上清液mIFN-γ的產生。
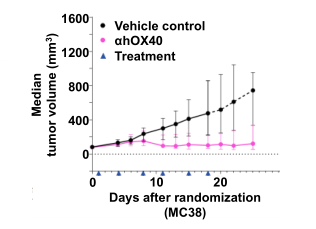
圖4. αhOX40在hOX40小鼠體內具有抗腫瘤活性。用αhOX40(BMS-986178類似物)處理移植了MC38腫瘤的hOX40小鼠。腫瘤的增殖明顯受到抑制。
小鼠腫瘤模型是研究腫瘤發生發展機制、藥物篩選及療效評價必不可少的工具,賽業生物模式動物創新藥物研發平臺還可以為您提供多種類型腫瘤模型,如BALB/c nude(裸鼠)、NOD scid、C-NKG和BRGSF等免疫缺陷鼠、免疫檢查點人源化小鼠、腫瘤細胞系移植模型、人源腫瘤組織異種移植模型(PDX)、基因修飾模型及表型分析服務,如有需要,歡迎聯系我們~
- 贊德公司關于美國Med associaties中國獨家代理聲明
- MCE推出AI藥物篩選平臺,實現數千萬的分子快速篩選
- 迪必爾入選2025關鍵技術研發計劃"合成生物學"項目
- 美國國立衛生研究院宣布停止對僅動物研究的資助
- 智聽自然,聲動未來:沃德精準亮相"聲景中國"研討會
- 赫西智能高速冷凍離心機亮相央視"革新人工催產技術"
- 易科泰榮膺“SFAA 植物工廠應用十大優秀企業”稱號
- 百蓁生物推出一站式高精度HDX-MS分析服務
- 10x Chromium GEM-X動物及畜牧類研究獎勵計劃啟動
- 生物芯片空間多組學平臺再添一臺CosMx SMI成像系統
- PicoQuant顯微鏡助力開發高效單光子發射源二維材料
- 安捷倫與北師大共建大灣區污水流行病學聯合實驗室
- 客戶專訪:RAYPA培養基制備器使用心得與經驗分享
- 美森攜CTCC細胞庫與干細胞技術亮相東南大學高研院
- 赫西儀器參與起草國標《實驗室離心機》條例
- 南模生物HSC模型全新升級,并可參與現貨優惠活動
- 美國國立衛生研究院宣布停止對僅動物研究的資助
- 南模生物邀您共赴美國華人生物醫藥科技中國年會
- 集光講壇:10年基因編輯大牛講解Cre/loxP應用全攻略
- 南模直播:一作解讀帕金森病治療新靶點FAM171A2
- 南模生物與GTP研發中心正式簽署GTP合作推廣計劃
- 明迅生物自主研發TIGIT人源化小鼠模型重磅來襲
- 南模生物將攜多個動物模型最新研究成果亮相AACR年會
- 南模生物邀您相約華東第17屆實驗動物科學學術交流會
- 南模生物大/小鼠實驗操作線下培訓班第二輪報名通知
- 南模生物邀您相約第二屆自免藥物及療法論壇
- 高品質實驗爪蟾上新!北京海威磐石獲準進口非洲爪蟾
- 賽業直播:從退行性疾病小鼠模型到新型AAV遞送突破
- 南模講座預告:誘導多能干細胞(iPSC)技術及應用前景
- 賽業講座:免疫重建小鼠在腫瘤免疫治療研究中的應用






