c-MET靶點的特性及相關小分子抑制劑、雙抗和ADC藥物研發進展
c-MET 靶點自 1984 年被發現以來,經歷了漫長的發展歷程,近年來,由于基礎科研和臨床研究的諸多新的進展和發現讓c-Met靶向藥物的研發重新吸引了眾人目光。
c-MET 靶點的特性與癌癥關聯
c-MET 是由原癌基因編碼的蛋白質,能與配體 HGF 結合,激活 PI3K/AKT、RAS/ERK/MAPK、Wnt/β-catenin 等多條下游重要信號通路。在正常生理狀態下,這些信號通路對胚胎發育、細胞增殖和組織修復至關重要。然而,癌細胞卻利用這一機制,通過異常激活 c-MET 信號通路,促進腫瘤的發生和轉移。
在多種癌癥中,如非小細胞肺癌、胃癌、肝癌、乳腺癌等,都存在 c-MET 信號通路異常的現象。其異常激活主要表現為 c-MET 基因擴增、c-MET 基因突變(主要是 Exon14 突變)以及 c-MET 基因過表達,但在不同癌種中的具體機制存在差異。例如,胃癌和食管癌常出現 c-MET 基因擴增,且與 EGFR 抑制劑耐藥相關,但對 c-MET 抑制劑反應不佳;甲狀腺癌、結直腸癌等多種癌癥中存在 c-MET 配體蛋白過表達的情況,不過其對現有 c-MET 抑制劑不敏感;在 1%-4% 的非小細胞肺癌患者中會出現 c-MET 外顯子 14 跳躍突變(c-METex14),雖然突變比例不高,但由于肺癌患者基數龐大,這部分患者數量也不容小覷,圍繞 c-METex14 的藥物研發成為當下熱門。
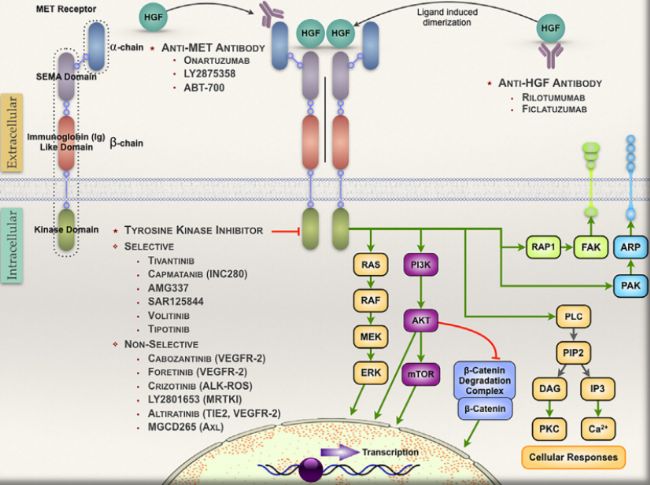
c-MET 小分子抑制劑
在 c-MET 抑制劑的研發進程中,小分子抑制劑率先取得突破。2011 年,輝瑞的多靶點 c-MET 抑制劑克唑替尼獲批上市,為 c-MET-14 跳躍突變的非小細胞肺癌患者帶來了新的希望。在此之前,這類患者接受鉑類化療的效果很差,緩解率極低,持續治療時間短。
克唑替尼的出現顯著改善了患者的生存率,在 PROFILE-1001 臨床試驗中,客觀緩解率達到 32%,中位無進展生存期達到 7.3 個月。此后,全球陸續有 7 款 c-MET 小分子抑制劑問世。根據作用原理和結合位點的不同,這些小分子抑制劑可分為 Ⅰ 類、Ⅱ 類、III 類。Ⅰ 類藥物主要作用于 c-MET 催化結構域,其中 Ⅰb 類單一激酶抑制劑如卡馬替尼、賽沃替尼、特泊替尼、谷美替尼等,能與 c-MET 蛋白獨特的鉸鏈區域結合,對 c-METex14 患者療效顯著,例如谷美替尼在所有患者中的客觀緩解率達到 60.9% 。Ⅱ 類藥物作用于調節性結構域,可用于對 Ⅰa 類藥物耐藥的患者,如卡博替尼可用于克唑替尼耐藥后的肺癌患者。III 類靶向活性形式的 c-MET 激酶,如默克的MK2461,雖酶活性高,但細胞活性不佳,臨床療效不明顯,已停止臨床開發。目前,除已獲批上市的產品外,國內眾多藥企也在積極研發 c-MET 抑制劑,未來該領域的競爭將愈發激烈。
c-MET 大分子藥物
相較于小分子抑制劑,c-MET 大分子藥物的研發之路充滿坎坷。c-MET 單抗理論上具有更好的靶向選擇性,但在實際研發中困難重重。羅氏的 onartuzumab 和安進的 Rilotumumab 在三期臨床試驗中均未達到預期效果,至今尚無 c-MET 單抗獲批上市。不過,c-MET 雙抗和 ADC 藥物的出現為大分子藥物研發帶來了轉機。2021 年 5 月,強生研發的 EGFR/c-MET 雙抗 Amivantamab 獲批上市,用于治療鉑類化療后進展的 EGFR 外顯子 20 插入突變的轉移性非小細胞肺癌患者。雙抗在應對 c-MET 小分子耐藥問題上具有獨特優勢,由于腫瘤細胞表面 c-MET 和 EGFR 距離相近,雙抗同時作用于這兩個靶點,有望解決耐藥難題。受此啟發,國內多家藥企如岸邁生物、貝達藥業、嘉和生物等紛紛布局 EGFR/c-MET 雙抗乃至多抗的研發。同時,c-MET ADC 藥物也逐漸成為研發熱點。截至今年 3 月,全球已有 15 款靶向 c-MET ADC 藥物在研,9 款進入臨床階段,艾伯維的 Teliso-v 已進入臨床 III 期。國內恒瑞醫藥的 SHR-A1403 早在 2018 年 5 月就已獲批臨床,是國內首個進入臨床階段的 c-MET ADC 藥物。
c-MET 靶點在抗癌藥物研發領域雖歷經波折,但如今已取得了顯著進展。小分子抑制劑、雙抗和 ADC 藥物等多種類型藥物的研發齊頭并進,為癌癥患者帶來了更多的治療選擇和希望。然而,研發過程中仍面臨諸多挑戰,如進一步提高藥物的療效、克服耐藥性、降低副作用等。隨著研究的不斷深入和技術的持續創新,相信 c-MET 靶點在未來抗癌治療中將會發揮更大的作用,為攻克癌癥這一難題提供有力支持。
產品信息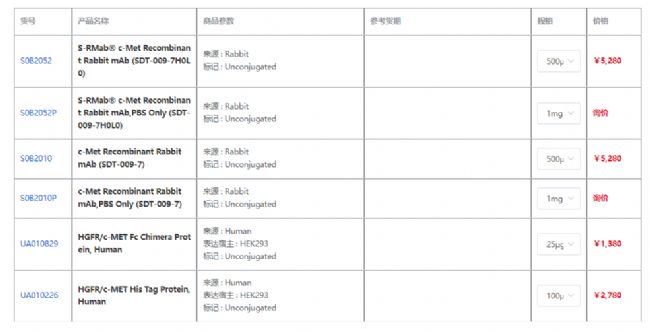
杭州斯達特 (www.starter-bio.com)志在為全球生命科學行業提供優質的抗體、蛋白、試劑盒等產品及研發服務。依托多個開發平臺:重組兔單抗、重組鼠單抗、快速鼠單抗、重組蛋白開發平臺(E.coli,CHO,HEK293,InsectCells),已正式通過歐盟98/79/EC認證、ISO9001認證、ISO13485。
參考文獻
[1] Paolo M. Comoglio, Silvia Giordano andLivio Trusolino. Drug development of MET inhibitors: targeting oncogeneaddiction and expedience. doi: 10.1038/nrd2530.
[2] Comoglio PM, Trusolino L, Boccaccio C.Known and novel roles of the MET oncogene in cancer: a coherent approach totargeted therapy. doi: 10.1038/s41568-018-0002-y.
[3] Zu-Jun Sun, Yi Wu, Wei-Hua Hou,Yu-Xiong Wang, Qing-Yun Yuan, Hui-Jie Wang and Min Yu. A novel bispecific c-MET/PD-1antibody with therapeutic potential in solid cancer. doi:10.18632/oncotarget.16173.